18.07.2025
“EasyDream”
Гидрогель для перорального приема с пролонгированным высвобождением мелатонина, предназначенный для лечения болевого синдрома и ноктурии при интерстициальном цистите/синдроме болезненного мочевого пузыря.
Product monography
Яков Миркин, Виктор Коржиков-Влах, Глеб Ковалев
Можно купить здесь:
Для интерстициального цистита (ИЦ), синдрома болезненного мочевого пузыря характерны следующие симптомы:
-
- Боль в области мочевого пузыря, обычно усиливающаяся при его наполнении.
- - Частое мочеиспускание в дневное время (поллакиурия).
- - Частое мочеиспускание в ночное время.
Хотя эти симптомы схожи с симптоматикой гиперактивного мочевого пузыря (ГМП), стандартная терапия ГМП обычно не приводит к улучшению состояния пациента [1].
ИЦ все еще остается диагнозом исключения, то есть может выставляться при исключении других патологических состояний со схожими симптомами. Для объективизации жалоб при подозрении на ИЦ полезны следующие диагностические инструменты:
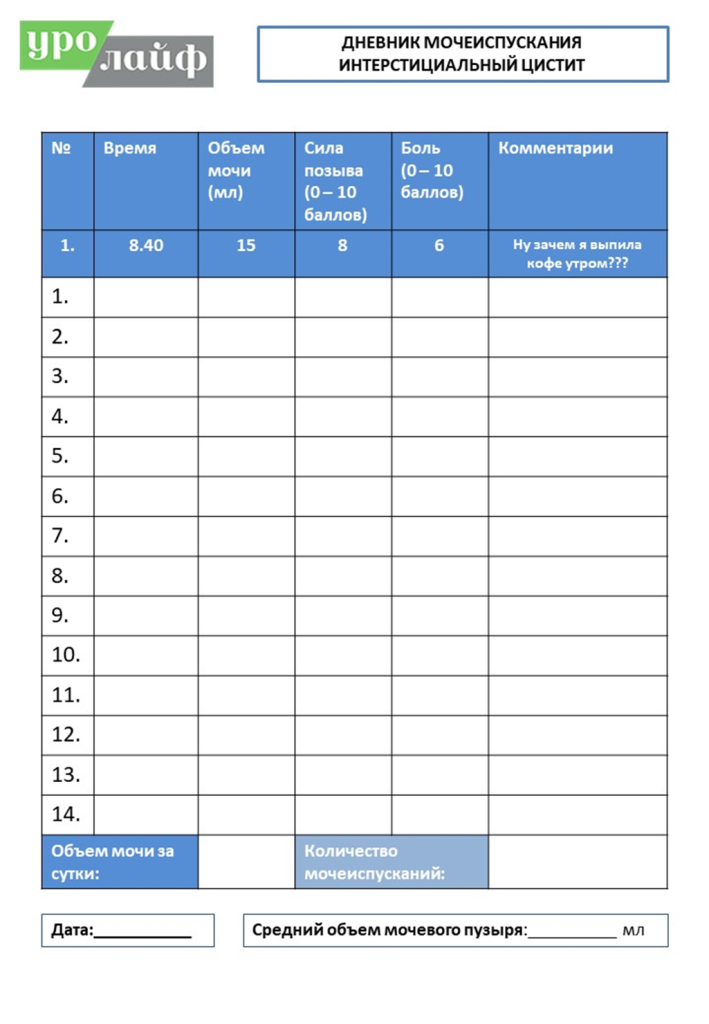
- Дневник мочеиспускания (Приложение 1)
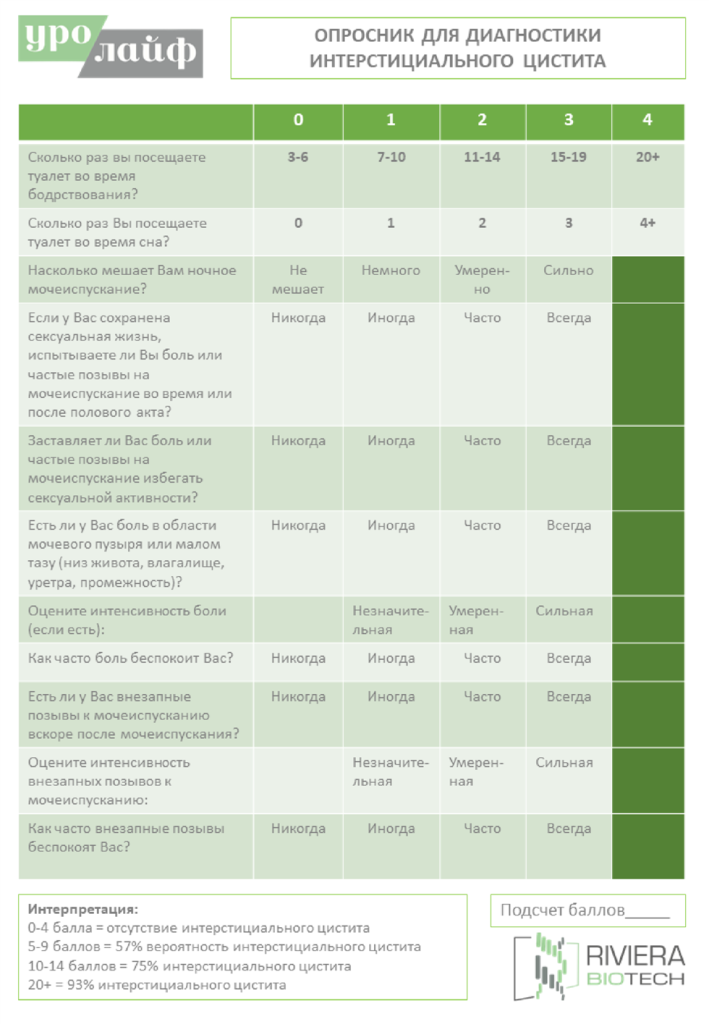
- Опросник PUF (Приложение 2)
- Визуальная Аналоговая Шкала симптомов ИЦ (Приложение 3)
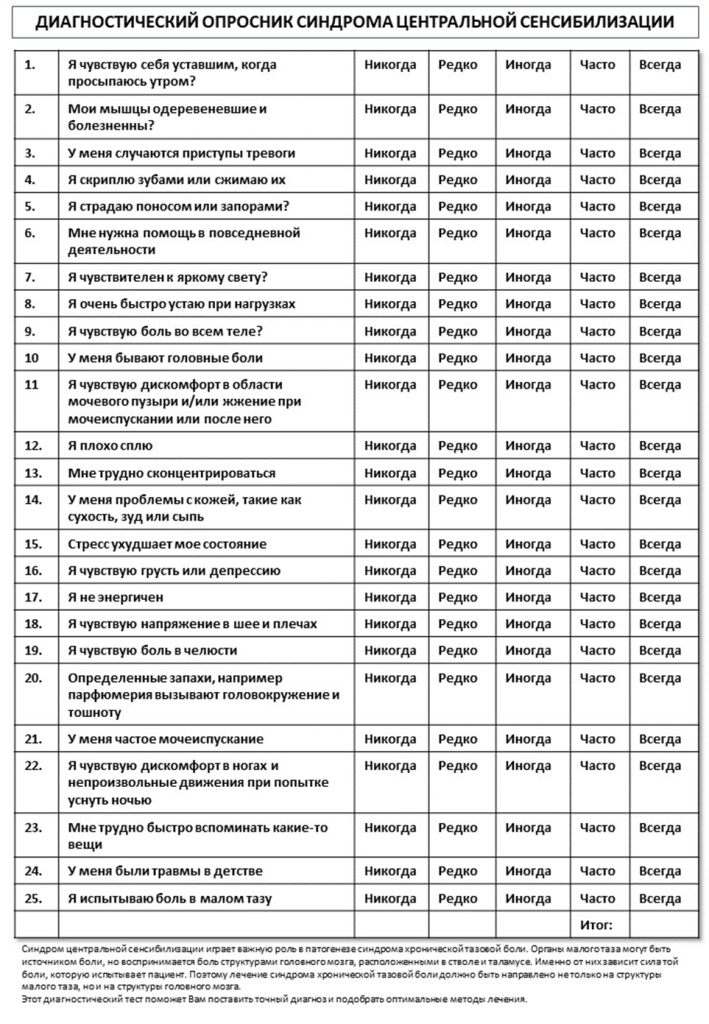
- Опросник Центральной Сенситизации (Приложение 4)
- Дневник сна (Приложение 5)
Для ИЦ характерны определенные изменения при цистоскопии:
- Гуннеровское поражение при язвенной форме интерстициального цистита.
- Подслизистые кровоизлияния (т.н. гломеруляции), визуализируемые при цистоскопии с гидродистензией мочевого пузыря – при неязвенной форме ИЦ.
Основное негативное влияние на качество жизни пациентов, страдающих ИЦ оказывают боль и ноктурия [2].
Влияние боли на качество жизни многократно описано и не вызывает сомнений. Однако, влияние нарушения сна тоже не следует недооценивать [3,4]
Таким образом, с точки зрения симптоматической терапии ИЦ, необходим препарат, который бы обладал анальгетической активностью и при этом оказывал позитивное влияние на глубину и продолжительность т.н. непрерывного сна. В рамках данной монографии мы рассмотрим возможность применения мелатонина в качестве препарата для симптоматической и в известной мере патогенетической терапии ИЦ.
Анальгетическая эффективность мелатонина
Существует много работ, подтверждающих анальгетический эффект мелатонина как в экспериментах на животных, так и в клинической практике.
Например, Esposito и соавторы опубликовали работу, демонстрирующую снижение гипералгезии, ассоциированной с воспалением. Крысам выполнялась инъекция пероксинитрита субплантарно.
Мелатонин (25-100 мг/кг, вводимый внутрибрюшинно за 30 мин до инъекции) дозозависимо ослаблял гипералгезические реакции на пероксинитрит . Более того, мелатонин (100 мг/кг) значительно уменьшал повреждение тканей и воспаление, ингибировал циклооксигеназу-2, и экспрессию синтазы оксида азота в тканях лапы [5]. Golombek продемонстрировал, что внутрибрюшинное введение 20 -40 мг/кг мелатонина мышам оказывало значительный анальгетический эффект в тесте с горячей пластиной, особенно в темное время суток [6].
Mantovani опубликовала результаты исследования взаимодействия мелатонина и NMDA-рецепторов. В этом исследовании изучалось влияние мелатонина в тесте подвешивания за хвост у мышей (ТПХ) и вклад рецепторов N-метил-D-аспартата (NMDA) и пути L-аргинин-оксид азота (NO) в его антидепрессантоподобный эффект. Время неподвижности в ТПХ сокращалось при введении мелатонина интраперитонеально (0,1-30 мг/кг). Более того, субэффективная доза мелатонина (0,001 мг/кг, интраперитонеально) произвела синергический антидепрессантоподобный эффект с MK-801, кетамином, хлоридом цинка и имипрамином в ТПХ. В совокупности эти данные указывают на то, что эффект мелатонина в ТПХ, повидимому, опосредован взаимодействием с рецепторами NMDA и путем Lаргинин-NO [7]. Tu опубликовал статью по исследованию влияния мелатониновых МТ-2 на капсаицин-индуцированную гипералгезию. Его результаты предполагают, что активация эндогенной системы мелатонина в спинном мозге может уменьшить генерацию, развитие и поддержание центральной сенсибилизации, что приводит к ингибированию вызванной капсаицином вторичной механической аллодинии и гипералгезии [8]. Yu исследовал антиноцицептивный эффект мелатонина у крыс, который определялся по латентности отдергивания хвоста в ответ на горячую воду при температуре 50 градусов по Цельсию. При внутрибрюшинном введении мелатонин (30, 60 и 120 мг/кг) оказывал дозозависимый антиноцицептивный эффект с A(50) 72,8 мг/кг.
Обнадеживающие результаты экспериментов на животных не вполне подтвердились в клинических исследованиях на людях. В частности, Lisa Sodermann исследовала эффективность мелатонина в лечении боли, ассоциированной с эндометриозом.
Это рандомизированное двойное слепое плацебо-контролируемое исследование не смогло показать, что 20 мг мелатонина, принимаемого перорально перед сном, имели лучший анальгетический эффект при боли, связанной с эндометриозом, по сравнению с плацебо. Неблагоприятных эффектов, правда не наблюдалось [10].
Индийские ученые исследовали эффективность мелатонина при СРК в плацебо-контролируемом исследовании, правда всего с 9 участниками в основной и 9-ю – в группе плацебо. Эффективность мелатонина (3 мг) была статистически значимо выше, чем плацебо [11].
De Zanette и соавторы исследовали эффективность мелатонина при фибромиалгии. В этом исследовании 63 женщины были разделены на 3 группы:
- Амитриптилин 25 мг
- Мелатонин 10 мг
- Амитриптилин 25 мг + мелатонин 10 мг
Оценивался балл боли по визуальной аналоговой шкале (ВАШ 0-100 мм), балл по опроснику воздействия фибромиалгии (FIQ), температурный болевой порог, качество сна и уровень BDNF в плазме. В этом 6-недельном рандомизированном, двойном плацебоконтролируемом исследовании мелатонин отдельно или в сочетании с амитриптилином был эффективнее, чем амитриптилин отдельно в плане улучшении боли по ВАШ, FIQ. Мелатонин увеличил активность ингибирующей эндогенной системы модуляции боли. Кроме того, это исследование позволяет предположить, что периферический BDNF можно использовать в качестве биомаркера центральной сенсибилизации, поскольку он обратно коррелирует со снижением боли [12].
Zhang и соавторы исследовали влияние мелатонина на симптомы и патогенез интерстициального цистита, вызванного введением циклофосфамида. У подопытных крыс измерялась частота мочеиспускания, на 7й день мочевой пузырь удалялся для гистологического исследования, в том числе определения уровня SP. У крыс, получавших мелатонин, симптомы циклофосфамидного цистита проявлялись менее выраженно. Воспалительные изменения в мочевом пузыре, так же как уровень SP были значительно меньше в группе мелатонина [13].
Из приведенных данных мы можем увидеть, что наибольший эффект терапия мелатонином оказывает на пациентов с патологией, коморбидной к ИЦ и сопровождающейся центральной сенситизацией. Однако, существуют исследования, демонстрирующие прямое влияние мелатонина на мочевой пузырь. В исследовании Ramsay доказано, что экзогенно принимаемый мелатонин может подавлять механочувствительность низкопороговых мышечно-слизистых афферентов через рецепторы MT2, сопряженные с Gбелком и улучшать возрастные изменения сократимости мочевого пузыря благодаря своим антиоксидантным свойствам [14].
Существует несколько работ, демонстрирующих эффективность мелатонина при ноктурии. Известно, что активность детрузора и чувствительность афферентных нервных окончаний мочевого пузыря подвержена циркадным ритмам и снижается в ночное время под влиянием мелатонина [15]. Sugaya и соавторы отметили снижение ноктурии у пожилых пациентов при назначении 2 мг мелатонина перед сном [16]. M.Drake изучал эффективность 2 мг мелатонина с замедленным высвобождением у пациентов с ноктурией и ДГПЖ. Результаты в группе мелатонина были лучше, чем в группе плацебо, но незначительно [17].
ВЛИЯНИЕ МЕЛАТОНИНА НА МОЧЕВОЙ ПУЗЫРЬ
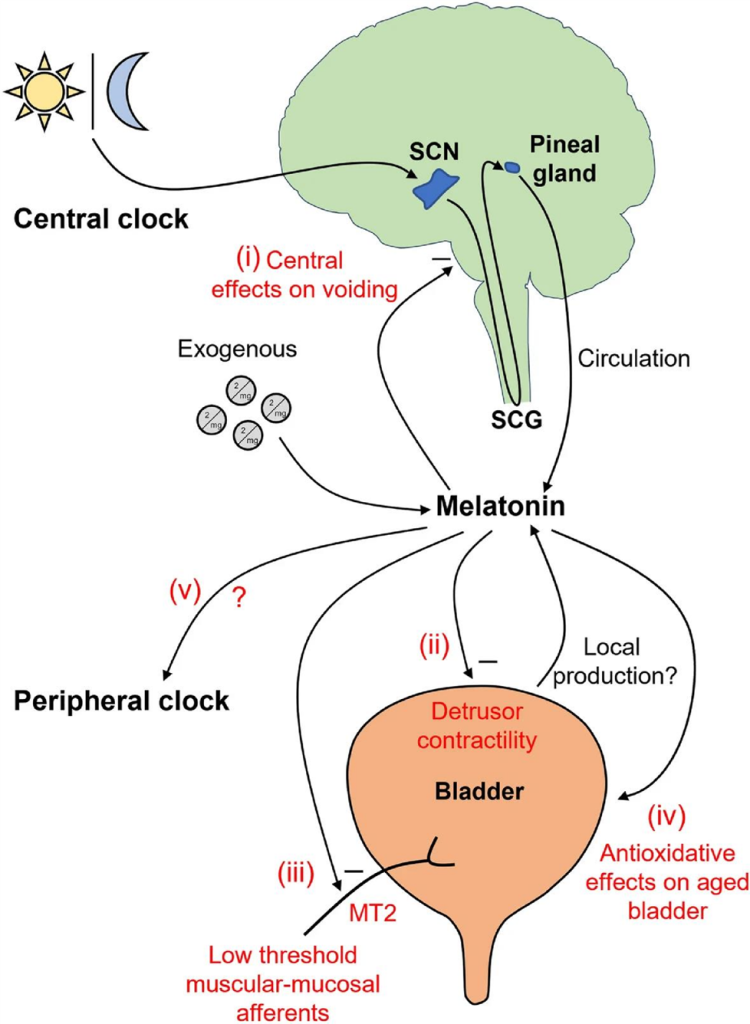
Итак, из приведенных данных следует, что мелатонин эффективен в качестве анальгетика центрального действия, так же он влияет на чувствительность афферентных волокон мочевого пузыря, особенно в ночное время суток. Это делает мелатонин весьма перспективным препаратом для лечения основных симптомов интерстициального цистита/синдрома болезненного мочевого пузыря.
Однако, есть определенные нюансы, которые затрудняют внедрение мелатонина в клиническую практику:
- Необходимость подбора дозы, с постепенным ее увеличением.
- Необходимость длительного действия, на протяжении 7 – 8 часов.
Основная проблема приема мелатонина — короткое время его действия. После перорального приема пик концентрации в плазме возникает в течение 60 минут [18]. Уменьшение концентрации в плазме происходит в два этапа, с периодом полувыведения соответственно 2 и 20 минут [19]. Исследование биодоступности у четырех здоровых добровольцев мужского пола показало, что пик мелатонина в плазме варьируется от 2 до 395 нмоль/л, а период полувыведения составляет 47±3 мин (среднее значение ± SD) после перорального приема дозы 500 мкг. [20].
В Израиле выпускается мелатонин с замедленным высвобождением в виде таблеток дозировкой 2 мг. Исходя из экспериментов на животных – такой дозы абсолютно недостаточно для лечения болевого синдрома при ИЦ. Мы решили разработать мелатонин замедленного высвобождения в виде гидрогеля для перорального приема. Основными преимуществами такой формы выпуска являются:
- Возможность постепенного увеличения дозы с ее точным подбором.
- Продолжительность действия 7 - 9 часов.
МЕЛАТОНИН ЗАМЕДЛЕННОГО ВЫСВОБОЖДЕНИЯ В ВИДЕ ГИДРОГЕЛЯ ДЛЯ ПРИЕМА ВНУТРЬ
Торговое наименование: «ИзиДрим» (“EasyDream”)
Форма выпуска: гидрогель на базе коньюгата пектина и гиалуроновой кислоты, 250 мл в флаконе
Состав (в 5 мл):
|
- |
Мелатонин |
– 5 мг |
|
- |
Магния глицинат |
– 750 мг |
|
- |
Витамин В6 |
– 5 мг |
|
- |
GABA |
– 375 мг |
- Экстракт Зверобоя
- Экстракт Пиона
- Экстракт Душицы
- Экстракт Чабреца
- Экстракт Иван-чая
Показания к применению:
- Лечение нарушений сна
- Лечение болевого синдрома при интерстициальном цистите
- Лечение ноктурии
Способ применения:
- Начало терапии – 5 мл за 1 – 1.5 часа до сна
- При недостаточном эффекте – 10 мл
- Далее повышается доза на 5 мл каждый день, до достижения эффекта.
- Максимальная доза – 50 мл
“EasyDream” мелатонин замедленного высвобождения на базе гидрогеля
Основное преимущество: замедленное высвобождение мелатонина в течение 7-9 часов.
Выбор пектина и гиалуроновой кислоты в качестве основы для гидрогеля основывался на данных литературы [21, 22] и собственных исследованиях invitro на базе Института Химии СПбГУ.
Сравнивали профиль высвобождения мелатонина, упакованного в гидрогели на базе пектина, гиалуроновой кислоты, альгината натрия.
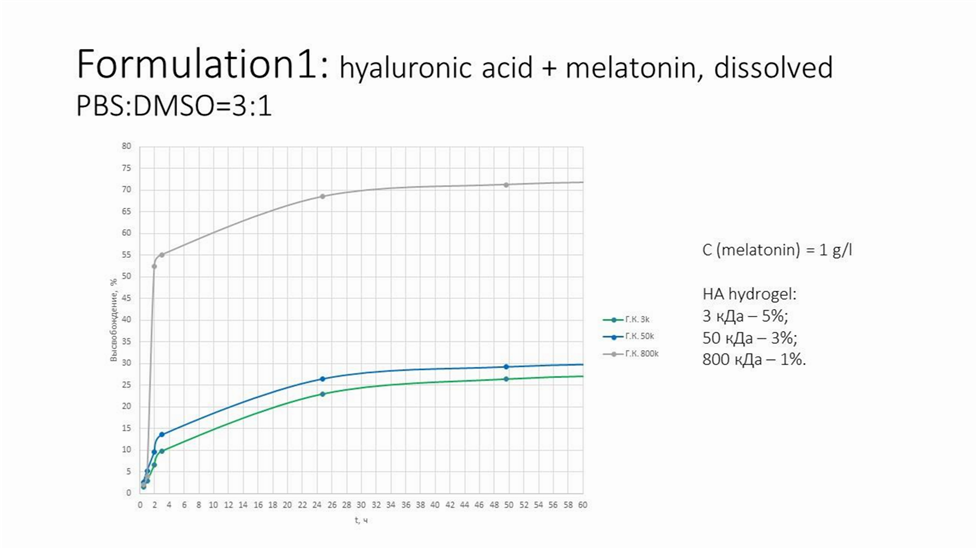
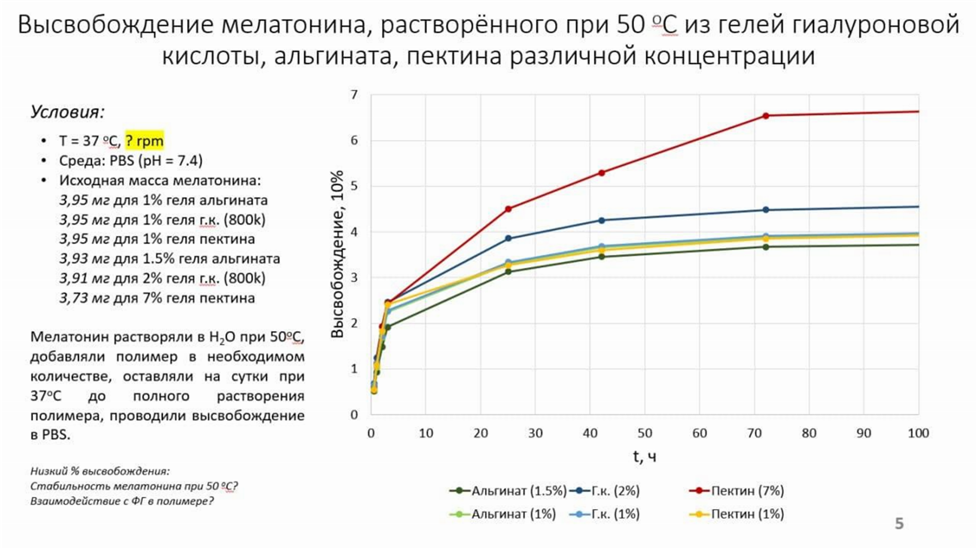
После определения профиля высвобождения мелатонина in vitro, был проведен эксперимент на животных в виварии КубГМУ. Целью эксперимента было определение анальгетического эффекта гидрогеля с мелатонином и продолжительности его действия in vivo.
ЭКСПЕРИМЕНТ НА ЖИВОТНЫХ
Эксперимент с крысами (тест отдергивания хвоста при погружении в горячую воду) продемонстрировал существенную разницу между группой плацебо и группой мелатонина: 10 мг/1 кг массы тела крысы: 7-секундная латентность отдергивания хвоста крысы в горячей воде (52 С) в контрольной группе и 15секундная латентность отдергивания хвоста в группе мелатонина. Этот эффект сохранялся в экспериментах на животных в течение 4,5 часов. Таким образом, мелатонин значительно повышает болевой порог. Поскольку известен дозозависимый антиноцицептивный эффект мелатонина, следует ожидать дальнейшего увеличения латентности при повышении дозы.
ПИЛОТНОЕ КЛИНИЧЕСКОЕ ИССЛЕДОВАНИЕ
Пилотное клиническое исследование в клинике URO-PRO показало эффективность «EasyDream» при ноктурии у пациентов с интерстициальным циститом/синдромом болезненного мочевого пузыря. Начальная доза составила 10 мг мелатонина.
В исследовании участвовали 12 женщин с неязвенной формой ИЦ (т.е. с синдромом болезненного мочевого пузыря). Перед началом исследования все участники заполняли дневник мочеиспускания в течении 3-х дней, анкету качества сна (приложение 6), дневник сна (приложение 7), Визуальную Аналоговую Шкалу симптомов ИЦ (ВАШ ИЦ УРО-ПРО).
Терапия начиналась с 10 мг мелатонина (10 мл гидрогеля “EasyDream”) за 1 – 1.5 часа до сна. На следующее утро пациентка заполняла дневник сна, ВАШ ИЦ, анкету качества сна.
Положительным результатом считалось:
- Достижение не менее 4-х баллов по каждому домену анкеты сна
- Продолжительность непрерывного сна до первого пробуждения не менее 3-х часов
- Количество ночных пробуждений не более 2-х.
В случае отсутствия указанных результатов доза “EasyDream” повышалась каждый день на 5 мл. Продолжительность исследования составляла 30 дней. На 28-й, 29-й и 30-й дни исследования участники заполняли дневник мочеиспускания.
Трое пациенток были выведены из исследования, т.к. нерегулярно заполняли документацию.
Результаты приведены ниже:
- Число мочеиспусканий в сутки уменьшилось с 19,89 до 9,33
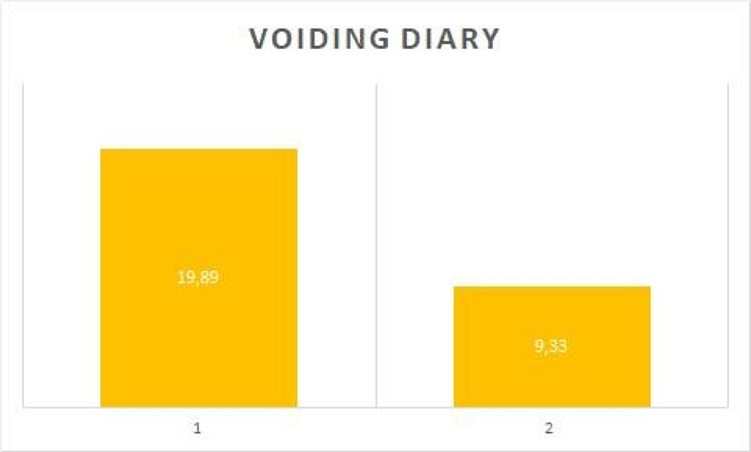
- Средний объем мочевого пузыря по данным дневника мочеиспускания увеличился с 82,11 мл до 170, 38 мл
- Время непрерывного сна до 1-го пробуждения увеличилось с 47,22 минут до 211,11 минут.
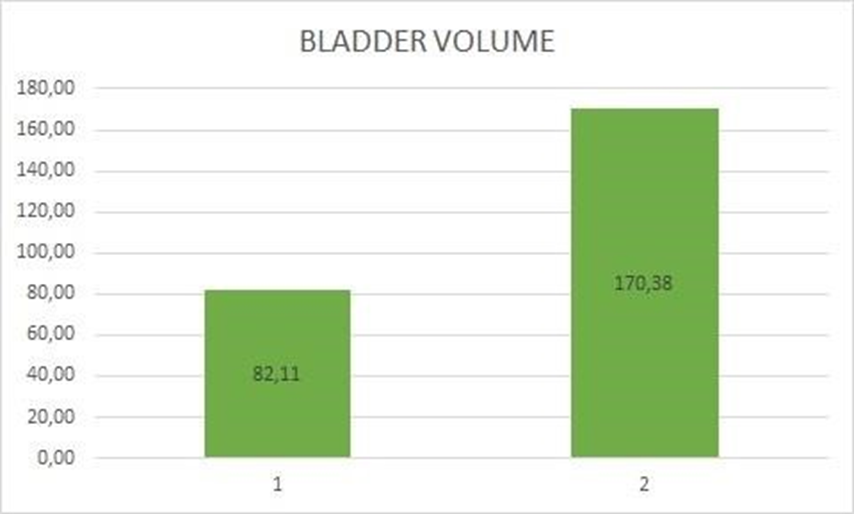
Средний объем мочевого пузыря: 1 – до, 2 – после.
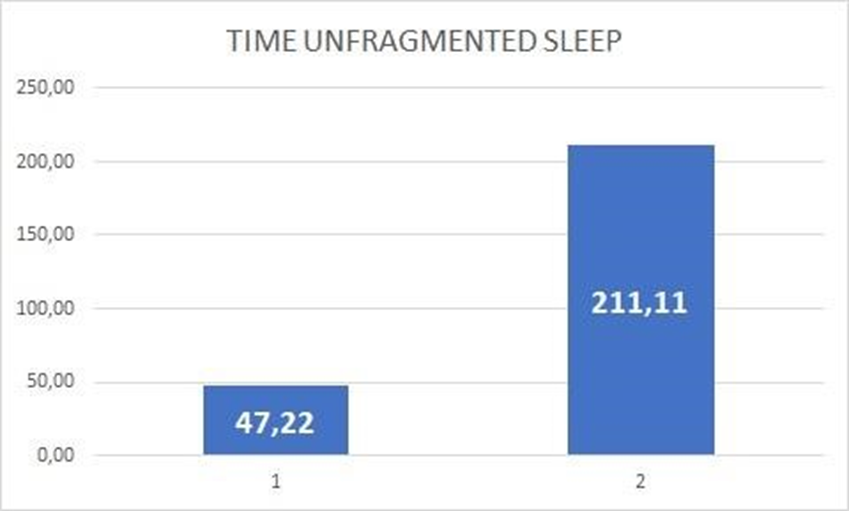
Время непрерывного сна до 1-го пробуждения: 1 – до, 2 - после
- Средняя доза мелатонина составила: 27 мг. (20 – 35 мг.), т.е. от 20 мл до 35 мл “EasyDream”
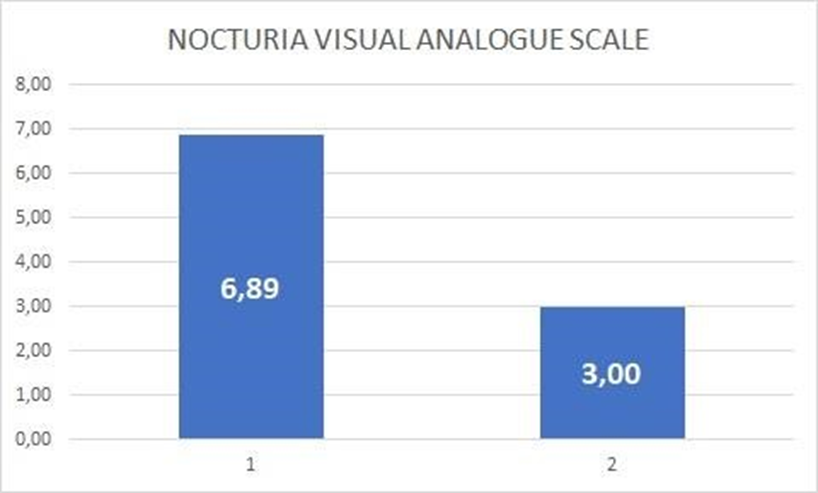
- Домен «Ноктурия» ВАШ ИЦ снизился с 6,89 до 3,00
- Домен «Боль» ВАШ ИЦ снизился с 6,22 до 3,11
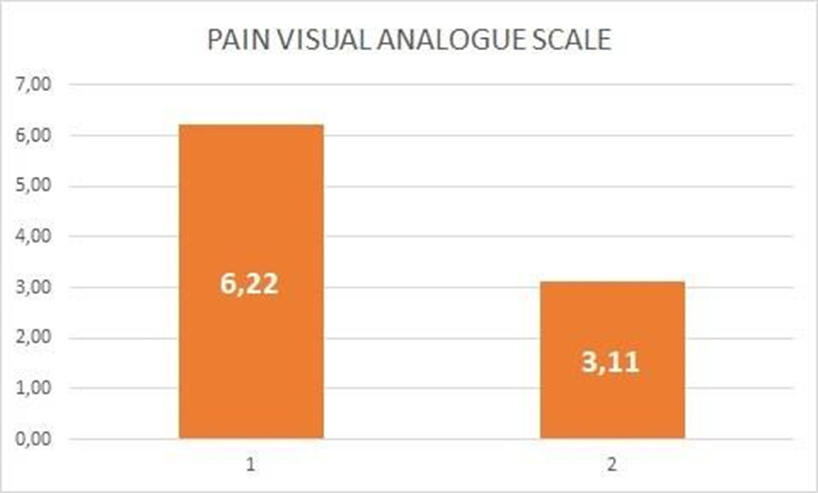
Исследование продемонстрировало высокую эффективность “EasyDream” в терапии болевого синдрома и ноктурии у пациентов с интерстициальным циститом/синдромом болезненного мочевого пузыря.
Таким образом, представляется перспективным использовать мелатонин замедленного высвобождения в качестве средства симптоматической и патогенетической терапии ИЦ/СБМП.
Способ применения:
- Начало терапии – 5 мл за 1 – 1.5 часа до сна
- При недостаточном эффекте – 10 мл
- Далее повышается доза на 5 мл каждый день, до достижения эффекта.
- Максимальная доза – 50 мл
СПИСОК ЛИТЕРАТУРЫ:
1. Lim Y, Leslie SW, O'Rourke S. Interstitial Cystitis/Bladder Pain Syndrome. 2024 Oct 7. In:
StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan–. PMID: 34033350.
2. Hetta J. The impact of sleep deprivation caused by nocturia. BJU Int. 1999 Dec;84 Suppl 1:27-
8. doi: 10.1046/j.1464-410x.84.s1.3 .x. PMID : 10674891.
3. Ancoli-Israel S, Bliwise DL, Nørgaard JP. The effect of nocturia on sleep. Sleep Med Rev. 2011 Apr;15(2):91-7. doi: 10.1016/j.smrv.2010.03.002. Epub 2010 Jun 8. PMID: 20965130; PMCID:
PMC3137590.
4. Miceli P. The prevalence of nocturia and its effect on health-related quality of life and sleep in a community sample in the USA. BJU Int. 2004 Jul;94(1):194-5. doi: 10.1111/j.1464410X.2004.4949 i.x. PMID : 15217468.
5. Esposito E, Paterniti I, Mazzon E, Bramanti P, Cuzzocrea S. Melatonin reduces hyperalgesia associated with inflammation. J Pineal Res. 2010 Nov;49(4):321-31. doi: 10.1111/j.1600079X.2010.00796 .x. PMID : 20666977.
6. Golombek DA, Escolar E, Burin LJ, De Brito Sánchez MG, Cardinali DP. Time-dependent melatonin analgesia in mice: inhibition by opiate or benzodiazepine antagonism. Eur J Pharmacol. 1991 Feb 26;194(1):25-30. doi: 10.1016/0014-2999(91)90119-b. PMID: 2060591.
7. Mantovani M, Pértile R, Calixto JB, Santos AR, Rodrigues AL. Melatonin exerts an antidepressant-like effect in the tail suspension test in mice: evidence for involvement of Nmethyl-D-aspartate receptors and the L-arginine-nitric oxide pathway. Neurosci Lett. 2003 May 29;343(1):1-4. doi: 10.1016/s0304-3940(03)00306-9 . PMID : 12749983.
8. Tu Y, Sun RQ, Willis WD. Effects of intrathecal injections of melatonin analogs on capsaicininduced secondary mechanical allodynia and hyperalgesia in rats. Pain. 2004 Jun;109(3):340350. doi: 10.1016/j.pain.2004.01.027. PMID : 15157695.
9. Yu CX, Zhu B, Xu SF, Cao XD, Wu GC. The analgesic effects of peripheral and central administration of melatonin in rats. Eur J Pharmacol. 2000 Sep 1;403(1-2):49-53. doi:
10.1016/s0014-2999(00)00421-0 . PMID : 10969143.
10. Söderman L, Böttiger Y, Edlund M, Järnbert-Pettersson H, Marions L. Adjuvant use of melatonin for pain management in endometriosis-associated pelvic pain-A randomized doubleblinded, placebo-controlled trial. PLoS One. 2023 Jun 2;18(6):e0286182. doi:
10.1371 /journal.pone.0286182. PMID: 37267394; PMCID: PMC 10237656.
11. Saha L, Malhotra S, Rana S, Bhasin D, Pandhi P. A preliminary study of melatonin in irritable bowel syndrome. J Clin Gastroenterol. 2007 Jan;41(1):29-32. doi:
10.1097 /MCG.0b013e31802df84c. PMID : 17198061.
12. de Zanette SA, Vercelino R, Laste G, Rozisky JR, Schwertner A, Machado CB, Xavier F, de Souza IC, Deitos A, Torres IL, Caumo W. Melatonin analgesia is associated with improvement of the descending endogenous pain-modulating system in fibromyalgia: a phase II, randomized, double-dummy, controlled trial. BMC Pharmacol Toxicol. 2014 Jul 23;15:40. doi: 10.1186/20506511-15-40 . PMID: 25052847; PMCID: PMC 4119581.
13. Zhang QH, Zhou ZS, Lu GS, Song B, Guo JX. Melatonin improves bladder symptoms and may ameliorate bladder damage via increasing HO-1 in rats. Inflammation. 2013 Jun;36(3):6517. doi: 10.1007/s10753-012-9588-5 . PMID : 23250825.
14. Ramsay, S., Zagorodnyuk, V. Melatonin inhibits muscular-mucosal stretch-sensitive bladder afferents via the MT2 receptors. Sci Rep 12, 17686 (2022). https://doi.org/10.1038/s41598-02222705-z
15. Negoro, H. et al. Involvement of urinary bladder Connexin43 and the circadian clock in coordination of diurnal micturition rhythm. Nat. Commun. 3, 809.
16. Sugaya K, Nishijima S, Miyazato M, Kadekawa K, Ogawa Y. Effects of melatonin and rilmazafone on nocturia in the elderly. J Int Med Res. 2007 Sep-Oct;35(5):685-91. doi:
10.1177/147323000703500513. PMID: 17900408.
17. Drake MJ, Mills IW, Noble JG. Melatonin pharmacotherapy for nocturia in men with benign prostatic enlargement. J Urol. 2004 Mar;171(3):1199-202. doi:
10.1097/01.ju.0000110442.47593 .ea. PMID : 14767300.
18. Waldhauser F, Saletu B, Trinchard-Lugan I. Sleep laboratory investigations on hypnotic properties of melatonin. Psychopharmacology (Berl). 1990;100(2):222-6. doi:
10.1007 /BF02244410. PMID : 2305009.
19. Claustrat B, Brun J, Chazot G. The basic physiology and pathophysiology of melatonin.
Sleep Med Rev. 2005 Feb;9(1):11-24. doi: 10.1016/j.smrv.2004.08.001. PMID : 15649735.
20. Di WL, Kadva A, Johnston A, Silman R. Variable bioavailability of oral melatonin. N Engl J
Med. 1997 Apr 3;336(14):1028-9. doi: 10.1056/NEJM199704033361418. PMID: 9091795.
21. Wang S, Cai J, Hu Y. [Research on hyaluronic acid and pectin complex]. Sheng Wu Yi Xue Gong Cheng Xue Za Zhi. 2009 Jun;26(3):561-5 . Chinese. PMID : 19634673.
22. Said NS, Olawuyi IF, Lee WY. Pectin Hydrogels: Gel-Forming Behaviors, Mechanisms, and Food Applications. Gels. 2023 Sep 9;9(9):732. doi: 10.3390/gels9090732. PMID:
37754413 ; PMCID: PMC 10530747.
ПРИЛОЖЕНИЕ 1
ПРИЛОЖЕНИЕ 2
ПРИЛОЖЕНИЕ 3

ПРИЛОЖЕНИЕ 4
ПРИЛОЖЕНИЕ 5

ПРИЛОЖЕНИЕ 6

НЕ ЯВЛЯЕТСЯ ЛЕКАРСТВЕННЫМ СРЕДСТВОМ
 Версия для слабовидящих
Версия для слабовидящих




